
Pietro Leone Germano
Chimico Industriale laureato all'Università di Padova. Mi piace insegnare e crescere insieme alle persone che mi circon…

Le batterie agli ioni di litio rappresentano oggi il cuore energetico degli smartphone. La loro diffusione è il risultato di un’evoluzione chimica e tecnologica che ha cercato un equilibrio tra densità energetica, durata e sicurezza.
Per comprenderle in modo completo, partiamo dai principi di funzionamento, analizziamo i parametri tecnici fondamentali e poi esaminiamo le principali tecnologie al litio sviluppate nel tempo.
Principi di funzionamento di una batteria
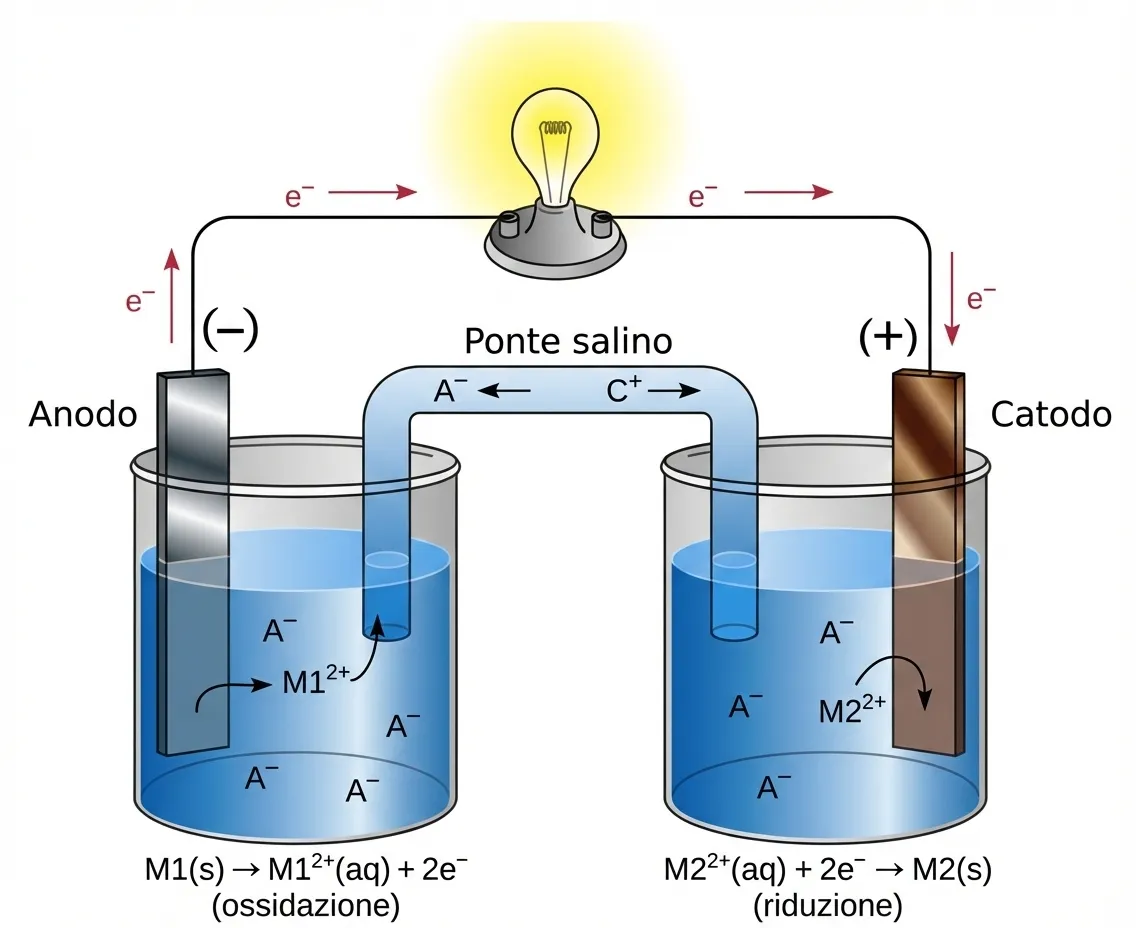
Una batteria è una cella elettrochimica che converte energia chimica in energia elettrica tramite una reazione di ossido-riduzione. È costituita da un anodo, un catodo e un un elettrolita che consente il trasporto ionico.
Durante la scarica, all’anodo avviene l’ossidazione con liberazione di elettroni; questi percorrono il circuito esterno alimentando il dispositivo. Contemporaneamente, gli ioni migrano attraverso l’elettrolita verso il catodo, dove avviene la riduzione. La corrente elettrica è quindi il risultato del flusso elettronico esterno, mentre il flusso ionico interno mantiene l’equilibrio di carica.
Durante la ricarica il processo si inverte: un generatore esterno forza il ritorno degli ioni alla configurazione iniziale, ripristinando lo stato chimico della batteria.
Parametri tecnici fondamentali
La qualità di una batteria si valuta attraverso alcuni parametri chiave.
La densità energetica (Wh/kg) indica quanta energia può essere immagazzinata per unità di massa. Nei moderni smartphone i valori tipici sono compresi tra 150 e 250 Wh/kg. Un valore elevato garantisce maggiore autonomia, ma implica anche una maggiore concentrazione di energia, con possibili implicazioni sulla sicurezza termica.
La profondità di scarica ("Depth of Discharge", DoD) rappresenta la percentuale di capacità utilizzata in ogni ciclo. Cicli con DoD elevata aumentano lo stress elettrochimico e riducono la vita utile complessiva.
L’efficienza coulombica, generalmente superiore al 99% nelle batterie al litio moderne, misura il rapporto tra carica restituita e carica immagazzinata. Valori elevati indicano basse perdite energetiche e ridotta produzione di calore.
Infine, la stabilità termica è un parametro cruciale: un’eccessiva generazione di calore può portare a fenomeni di instabilità come il "thermal runaway", un processo di surriscaldamento incontrollato che può provocare incendi e potenziali esplosioni.

Evoluzione delle tecnologie al litio
Batterie al litio di prima generazione
La prima tipologia di batterie al litio utilizzano litio metallico come anodo e biossido di manganese (MnO₂) come catodo,
Questa configurazione garantisce una buona densità energetica. Tuttavia, il litio metallico è altamente reattivo e durante i cicli di ricarica si possono formare dendriti capaci di perforare il separatore, aumentando il rischio di cortocircuiti interni.
La sicurezza risulta quindi il principale limite di questa tecnologia.
Batterie ai polimeri di litio
Per migliorare la stabilità del sistema, si sono sviluppate batterie ai polimeri di litio con elettrolita polimerico, spesso basato su PEO (polietilene ossido). Per questa tipologia l’anodo è di litio metallico, mentre il catodo è costituito da ossidi di litio.
L’introduzione del polimero ha ridotto il rischio di perdite di elettrolita liquido e ha migliorato l’integrazione meccanica nei dispositivi sottili. Tuttavia, la conducibilità ionica dei polimeri solidi è generalmente inferiore rispetto a quella degli elettroliti liquidi, rendendo necessaria una gestione termica ed elettronica più sofisticata del sistema.
Dal punto di vista della sicurezza, l’assenza di liquidi volatili rappresenta un miglioramento, ma la presenza di litio metallico continua a porre criticità legate alla formazione di dendriti.
Batterie al litio “Rocking Chair”
La vera svolta tecnologica è arrivata con le batterie agli ioni di litio “rocking chair”.
In questo sistema il litio non è più presente come metallo libero: gli ioni si intercalano reversibilmente nella grafite dell’anodo e negli ossidi metallici del catodo.
Durante la ricarica, le reazioni si invertono e gli ioni litio tornano a intercalarsi nella grafite.
Il meccanismo di intercalazione ha migliorato significativamente la sicurezza perché il litio non si deposita come metallo libero, riducendo drasticamente la formazione di dendriti. La grafite funge da struttura ospite stabile, consentendo cicli ripetuti con elevata efficienza.
Permangono comunque criticità legate a sovraccarica, alte correnti o temperature estreme, condizioni che possono portare alla deposizione di litio metallico o all’instabilità dell’elettrolita.
Per questo motivo gli smartphone integrano sistemi di Battery Management System (BMS) che controllano tensione, corrente e temperatura.
Oggi queste ultime rappresentano il miglior compromesso tra densità energetica, efficienza, durata e stabilità termica, rendendo possibile l’autonomia dei dispositivi mobili in condizioni di sicurezza controllata.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- 1) Nasajpour-Esfahani, N., Garmestani, H., Bagheritabar, M., Jasim, D. J., Toghraie, D., Dadkhah, S., & Firoozeh, H. (2024). Comprehensive review of lithium-ion battery materials and development challenges. Renewable and Sustainable Energy Reviews, 203, 114783. https://doi.org/10.1016/j.rser.2024.114783



