Francesco Sbalchiero
Professore di chimica industriale, chimica organica, chimica analitica, chimica inorganica, chimica-fisica. Proprietar…

Una delle domande più affascinanti e frequenti quando si studia la struttura della materia è la seguente: se l’elettrone ha carica negativa e il nucleo atomico è carico positivamente, perché l’elettrone non cade nel nucleo?
La risposta a questa domanda ci porta al cuore della fisica e della chimica moderna, in particolare alla meccanica quantistica.
Struttura dell’atomo e forza elettrostatica
Secondo il modello atomico attualmente accettato, l’atomo è composto da un nucleo centrale, contenente protoni (carica positiva) e neutroni (carica nulla), circondato da una nube elettronica formata dagli elettroni, che hanno carica negativa.
È noto fin dall’esperienza quotidiana che cariche di segno opposto si attraggono. Di conseguenza, l’elettrone dovrebbe essere attratto dal nucleo e, intuitivamente, ci si potrebbe aspettare che finisca per “precipitare” su di esso. Eppure, gli atomi sono stabili. Per comprenderne il motivo è necessario abbandonare la fisica classica e introdurre concetti quantistici.
Dai modelli planetari agli orbitali atomici
Nei primi modelli atomici, come quello proposto da Niels Bohr nel 1913 (Figura 1), l’elettrone veniva immaginato come una particella che orbitava attorno al nucleo in modo simile ai pianeti attorno al Sole. Sebbene questo modello sia oggi noto come incompleto e fisicamente scorretto, introdusse un’idea fondamentale: la quantizzazione dell’energia.

Secondo Bohr, solo alcune orbite erano permesse, ciascuna associata a un determinato valore di energia (Figura 2).
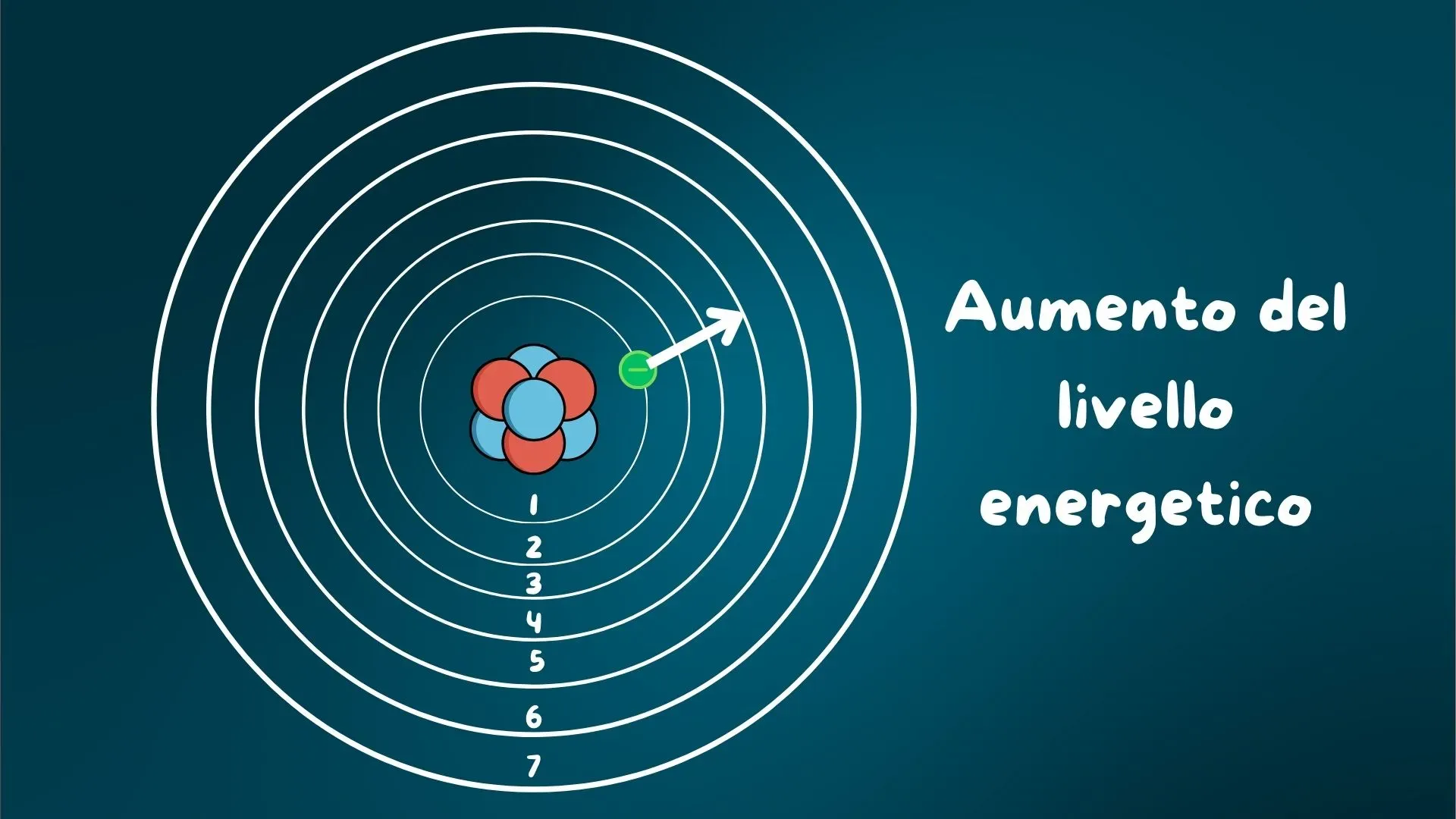
Questo concetto è sopravvissuto ed è stato raffinato dalla meccanica quantistica moderna, che ha sostituito le orbite con gli orbitali atomici.
Gli orbitali non sono traiettorie, ma regioni di spazio attorno al nucleo in cui è più probabile trovare l’elettrone. Essi hanno forme e dimensioni diverse e derivano direttamente dalle soluzioni dell’equazione di Schrödinger.
Livelli energetici quantizzati e spettroscopia
Uno degli aspetti fondamentali degli elettroni negli atomi è che essi possono possedere solo valori discreti di energia. In altre parole, l’energia dell’elettrone è quantizzata.
Un’analogia efficace è quella di una scala: un elettrone può trovarsi solo su determinati “gradini” energetici e non tra un gradino e l’altro. Quando passa da un livello energetico a un altro, assorbe o emette una quantità precisa di energia.
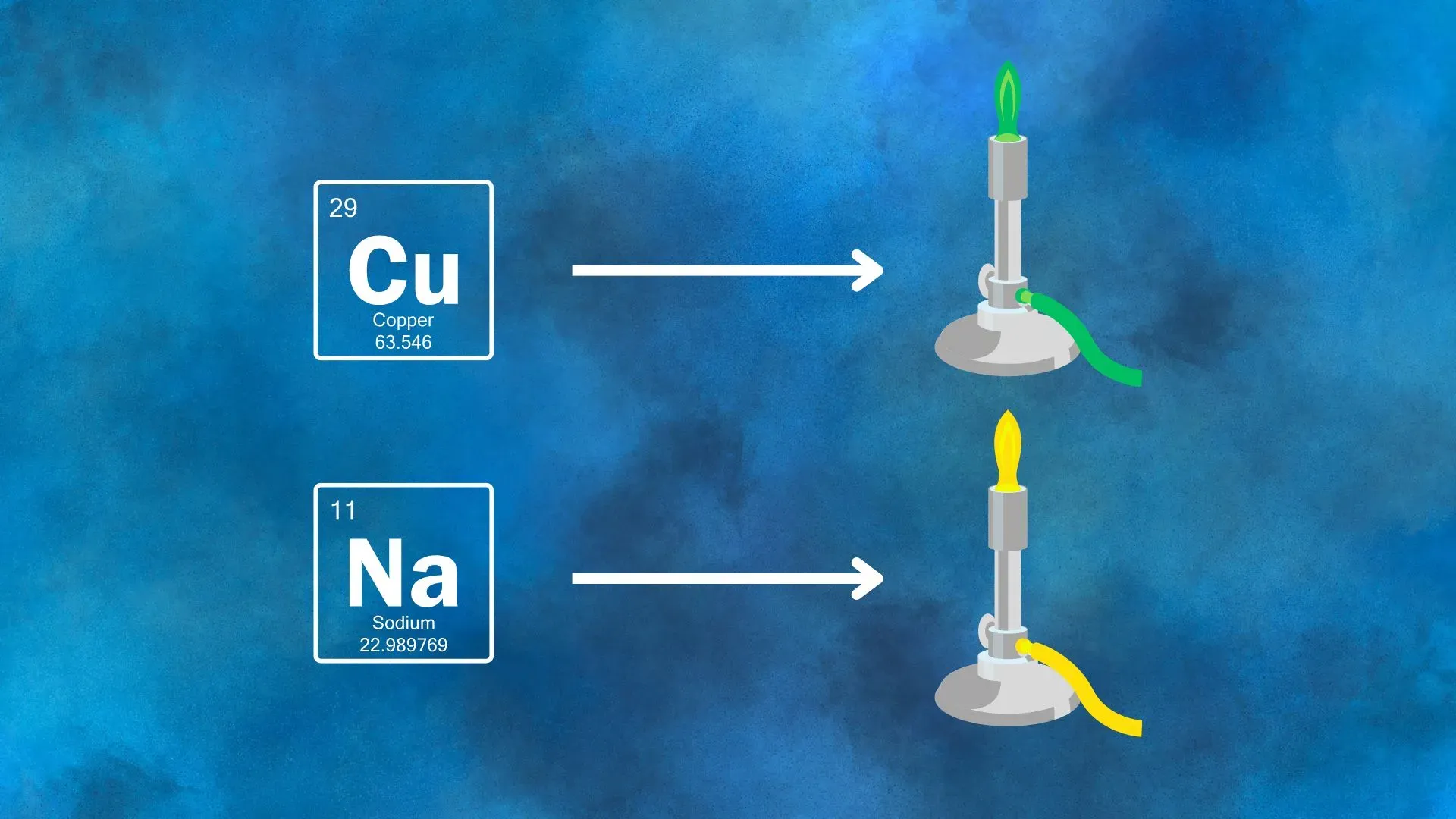
Questa quantizzazione è osservabile sperimentalmente, ad esempio nel saggio alla fiamma (Figura 3). Scaldando un elemento chimico, gli elettroni vengono eccitati a livelli energetici superiori. Tornando allo stato iniziale, emettono luce di lunghezze d’onda ben definite, responsabili dei colori caratteristici osservati (il sodio emette luce gialla, il rame verde, ecc.).
Questo fenomeno dimostra che i salti energetici sono discreti e specifici per ogni elemento.
Energia potenziale ed energia cinetica dell’elettrone
L’energia totale di un elettrone in un atomo è il risultato di due contributi principali:
-
energia potenziale elettrostatica, dovuta all’attrazione tra l’elettrone e il nucleo;
-
energia cinetica, legata al moto dell’elettrone.
L’energia potenziale elettrostatica dipende dalla distanza tra elettrone e nucleo ed è inversamente proporzionale ad essa. Più l’elettrone è vicino al nucleo, maggiore (in valore assoluto) è l’energia potenziale e più forte è il legame.
Se però l’elettrone fosse privo di energia cinetica, la sola attrazione elettrostatica lo farebbe collassare nel nucleo. La stabilità dell’atomo nasce quindi da un bilanciamento tra energia potenziale ed energia cinetica.
La descrizione quantistica: funzione d’onda e probabilità
Nella meccanica quantistica l’elettrone non segue una traiettoria ben definita. Il suo comportamento è descritto da una funzione d’onda ψ (Figura 4), soluzione dell’equazione di Schrödinger.
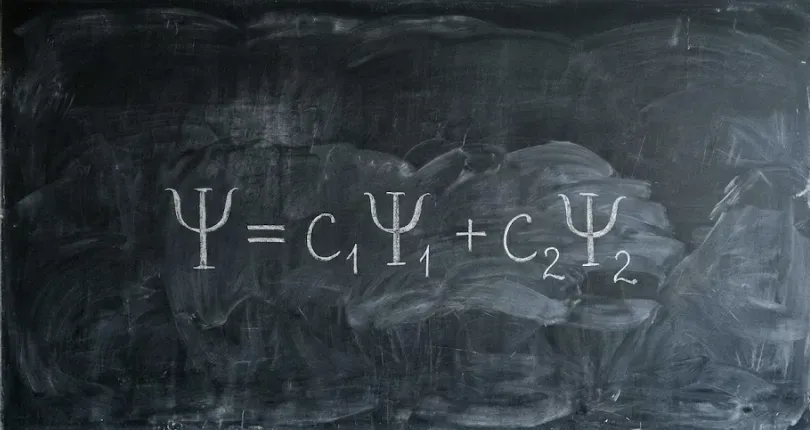
Il quadrato della funzione d’onda, |ψ²|, rappresenta la probabilità di trovare l’elettrone in una certa regione dello spazio (Figura 5).

Il fatto che l’elettrone sia confinato attorno al nucleo implica che esso possieda una energia cinetica minima, sufficiente a impedirne il collasso sul nucleo stesso.
Il principio di indeterminazione di Heisenberg
Un ulteriore elemento chiave è il principio di indeterminazione di Heisenberg (Figura 6), secondo il quale non è possibile conoscere simultaneamente con precisione arbitraria la posizione e la quantità di moto di una particella:
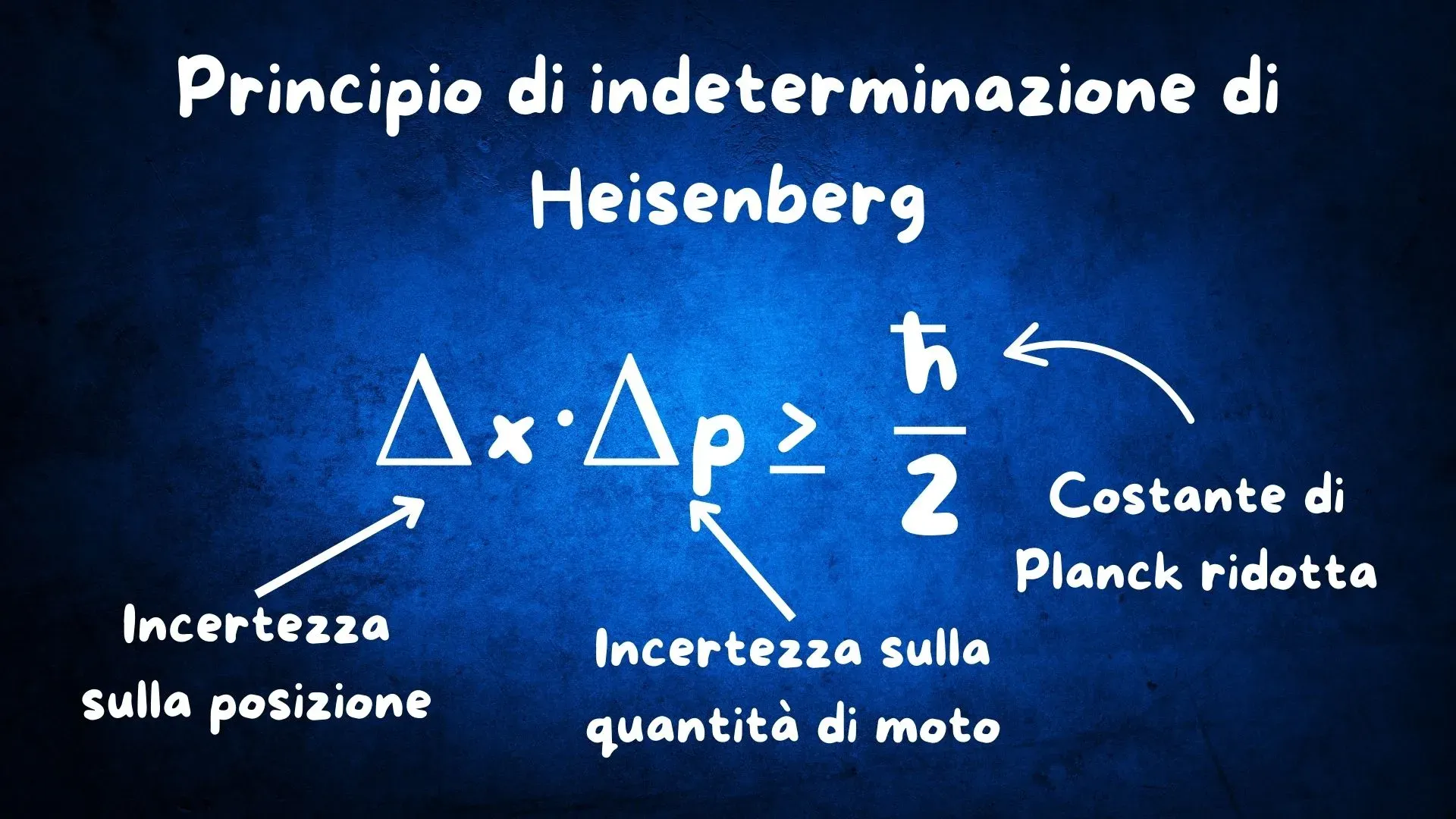
Questo significa che confinare l’elettrone in uno spazio sempre più piccolo (riducendo Δx) comporta un aumento dell’incertezza sulla sua quantità di moto e quindi della sua energia cinetica.
Ancora una volta, la fisica quantistica impedisce all’elettrone di collassare nel nucleo.
Un’analogia utile: i satelliti in orbita
Un paragone intuitivo è quello dei satelliti artificiali, come la Stazione Spaziale Internazionale (ISS). La gravità terrestre tende ad attirarla verso la Terra, ma la sua elevata velocità tangenziale le permette di restare in orbita. In questo caso, energia potenziale gravitazionale ed energia cinetica si bilanciano (Figura 7).
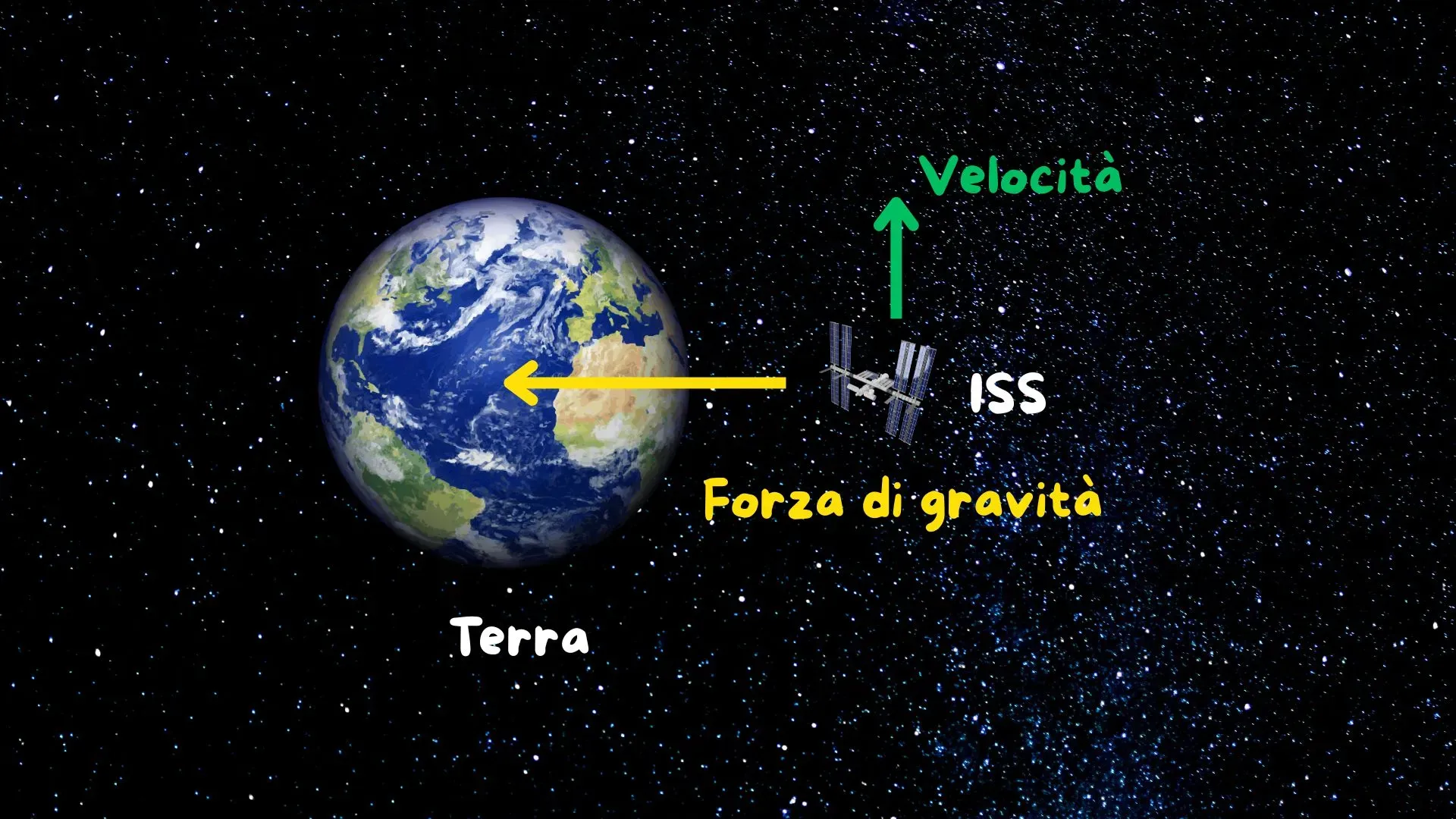
Con le dovute approssimazioni, si può pensare che l’elettrone si trovi in una situazione analoga: è soggetto a una forza attrattiva (elettrica anziché gravitazionale), ma il suo stato energetico e le leggi della meccanica quantistica ne impediscono il collasso.
Conclusione
Gli elettroni non cadono nel nucleo perché le leggi della meccanica quantistica lo impediscono. La quantizzazione dell’energia, il bilanciamento tra energia potenziale ed energia cinetica, la descrizione probabilistica tramite funzione d’onda e il principio di indeterminazione di Heisenberg rendono l’atomo una struttura stabile.
L’idea classica di elettroni che “orbitano” come pianeti è solo un’utile semplificazione: la realtà è molto più affascinante e profondamente quantistica.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- Video completo su YouTube (Frank explains): https://www.youtube.com/watch?v=Mi-FrhXTD9U