
Francesco Sbalchiero
Professore di chimica industriale, chimica organica, chimica analitica, chimica inorganica, chimica-fisica. Proprietar…
I composti binari dell’idrogeno rappresentano una classe fondamentale della chimica inorganica e comprendono tutte quelle sostanze formate dall’unione dell’idrogeno con un altro elemento.
La loro classificazione si basa principalmente sulla natura dell’elemento legato all’idrogeno e sul tipo di legame chimico che si instaura.
In particolare, è possibile distinguere tre grandi categorie:
-
Idruri salini
-
Idruri molecolari (o covalenti)
-
Idracidi
Questa distinzione non è solo formale, ma riflette profonde differenze strutturali, proprietà fisiche e comportamento chimico, rendendo essenziale una corretta comprensione per affrontare lo studio della nomenclatura e delle reazioni.
Idruri salini: struttura ionica e proprietà
Gli idruri salini sono composti che si formano quando l’idrogeno reagisce con metalli fortemente elettropositivi, in particolare quelli appartenenti ai gruppi I e II della tavola periodica, Figura 1.
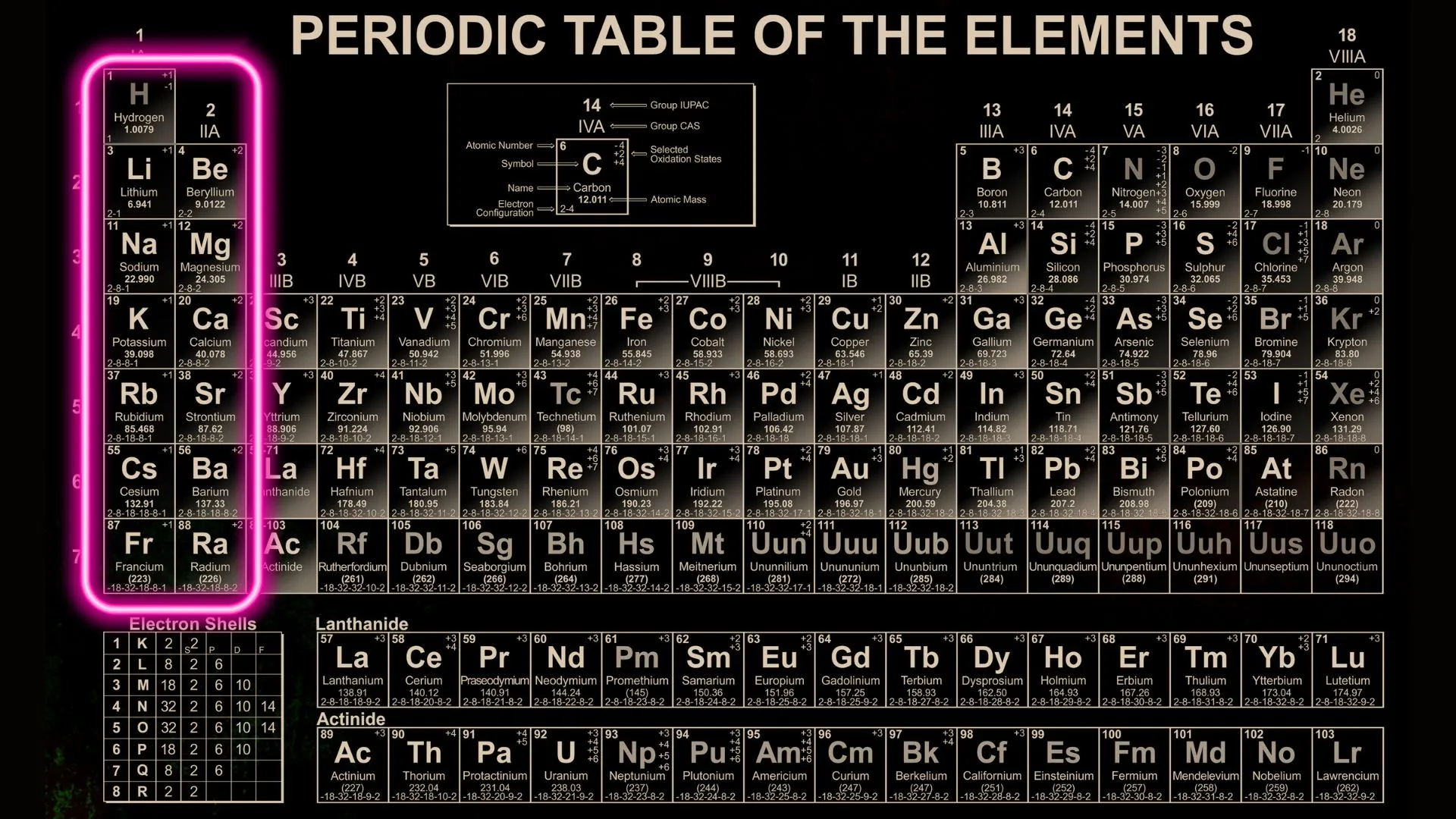
In questi composti, l’idrogeno assume il ruolo di anione sotto forma di ione idruro (H⁻), con numero di ossidazione pari a -1, mentre il metallo si comporta da catione. Ne risulta una struttura ionica simile a quella dei sali, da cui deriva il nome.
Dal punto di vista della scrittura delle formule, si segue la convenzione generale dei composti ionici: si indica prima il metallo e successivamente l’idrogeno (ad esempio LiH o CaH₂), Figura 2.
Questi composti si presentano tipicamente come solidi cristallini, con elevati punti di fusione e una marcata reattività, soprattutto nei confronti dell’acqua, con la quale liberano idrogeno gassoso.
Idruri molecolari: natura covalente e stato fisico
Gli idruri molecolari, detti anche idruri covalenti, si formano quando l’idrogeno si lega a non metalli o semimetalli, in particolare quelli dei gruppi IV, V e VI, Figura 3.
In questo caso il legame è di tipo covalente e porta alla formazione di molecole discrete, a differenza della struttura reticolare tipica degli idruri salini.
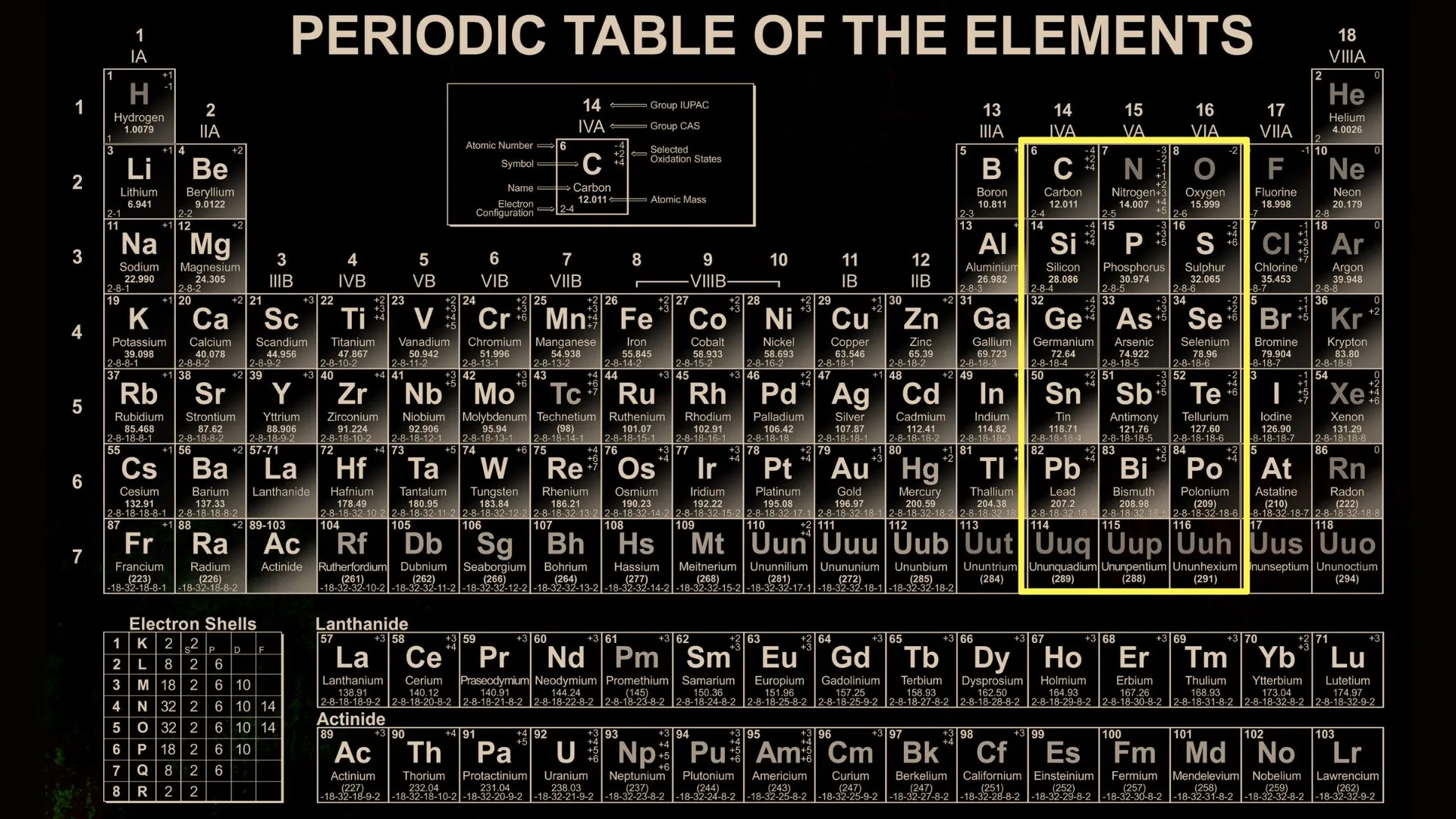
Dal punto di vista delle formule, anche qui si scrive prima l’elemento diverso dall’idrogeno e poi l’idrogeno stesso, come nel caso di CH₄ (metano) o NH₃ (ammoniaca).
Una caratteristica distintiva di questi composti è il loro stato fisico: molti sono gas o liquidi a temperatura ambiente, a causa delle forze intermolecolari relativamente deboli.
Le loro proprietà chimiche variano notevolmente a seconda dell’elettronegatività dell’elemento coinvolto e della geometria molecolare.
Nomenclatura degli idruri: IUPAC, tradizionale e Stock
La nomenclatura dei composti binari dell’idrogeno segue regole ben precise stabilite dalla IUPAC, ma nella pratica convivono anche nomenclature tradizionali e, in misura minore, quella di Stock.
Secondo la nomenclatura IUPAC, si utilizza il termine “idruro” preceduto da prefissi numerici (mono-, di-, tri-, tetra-) che indicano il numero di atomi di idrogeno, seguito dalla preposizione “di” e dal nome dell’elemento: ad esempio, tetraidruro di carbonio per CH₄.
Alcuni esempi sono riportati in Figura 4.
La nomenclatura tradizionale, invece, utilizza suffissi come -oso e -ico in funzione del numero di ossidazione dell’elemento centrale.
La nomenclatura di Stock indica esplicitamente tale numero tra parentesi in numeri romani. Tuttavia, per molti idruri molecolari sono ancora largamente utilizzati i nomi comuni (come metano e ammoniaca), il cui uso è ancora accettato.

Gli idracidi: comportamento acido e struttura
Gli idracidi costituiscono una particolare categoria di composti binari dell’idrogeno caratterizzati dalla presenza di un non metallo fortemente elettronegativo.
A differenza degli altri idruri, la loro formula viene scritta ponendo sempre l’idrogeno per primo (ad esempio HCl, HBr, HI).
La loro caratteristica principale è il comportamento acido in soluzione acquosa: quando vengono disciolti in acqua, si ionizzano liberando ioni H₃O⁺ (ioni idronio), responsabili dell’acidità della soluzione.
Questo comporta una diminuzione del pH e la capacità di modificare il colore degli indicatori acido-base. Gli idracidi sono spesso sostanze corrosive o irritanti e giocano un ruolo fondamentale sia in chimica teorica che in applicazioni industriali.
Nomenclatura degli idracidi: regole e esempi
La nomenclatura degli idracidi può seguire sia le regole IUPAC sia quelle tradizionali, entrambe ancora ampiamente utilizzate.
Secondo la IUPAC, si assegna al non metallo il suffisso “-uro”, seguito da “di idrogeno” (ad esempio cloruro di idrogeno o solfuro di diidrogeno).
La nomenclatura tradizionale, invece, è particolarmente diffusa e prevede l’uso del termine “acido” seguito dal nome del non metallo con il suffisso “-idrico”, come acido cloridrico, acido fluoridrico e acido iodidrico.
Un caso particolare è rappresentato dall’acido cianidrico (HCN), che pur contenendo tre elementi viene spesso incluso tra gli idracidi per le sue proprietà chimiche simili. Alcuni esempi sono riportati in Figura 5.

Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- Canale YouTube Frank Explains: https://www.youtube.com/watch?v=REhYo8m-SRI&list=PLG1-CnRdI8GJG7at6Krk3ay_ohb1o5vo5&index=8



