
Pietro Leone Germano
Chimico Industriale laureato all'Università di Padova. Mi piace insegnare e crescere insieme alle persone che mi circon…

Ogni sostanza, dai gas che respiriamo ai materiali più comuni come plastica, alimenti e bevande, è costituita da atomi che si combinano in molecole o in strutture più grandi. Per descrivere quantitativamente questi elementi microscopici, la chimica utilizza una grandezza fondamentale: il peso molecolare, o più correttamente massa molecolare.
Questa grandezza permette di collegare la composizione atomica di una sostanza alle sue proprietà chimiche, fisiche e applicative, e di capire come le molecole interagiscono tra loro sia in laboratorio sia nella vita quotidiana. Sapere la massa molecolare di acqua, zucchero o anidride carbonica ci permette di misurare correttamente le quantità in cucina, nella preparazione di bevande, negli esperimenti scolastici o persino nel calcolo della quantità di ossigeno che respiriamo.
Cos'è la massa molecolare?
La massa molecolare (comunemente nota come peso molecolare) è una grandezza chimica che indica la massa di una singola molecola.
Si ottiene facendo la somma delle masse atomiche di tutti gli atomi che compongono la formula chimica della sostanza, espressa in unità di massa atomica (u).
L’unità di massa atomica (u): una scala adatta agli atomi
La massa di un singolo atomo è estremamente piccola, dell’ordine di 10⁻²⁶ kg, e non sarebbe pratica da usare direttamente. Per rendere i numeri più gestibili, i chimici hanno definito l’unità di massa atomica (u): un dodicesimo della massa di un atomo di carbonio‑12 (C12).
-
Un atomo di idrogeno ha massa circa 1 u
-
Un atomo di carbonio 12 u
-
Un atomo di ossigeno pesa circa 16 u
L’unità di massa atomica è utile per confrontare tra loro atomi e molecole, ma in laboratorio non ci permette di pesare direttamente quantità pratiche di sostanza. Ad esempio, non possiamo pesare un singolo atomo di carbonio: i numeri sono troppo piccoli.
Grammi per mole (g/mol): dal microscopico al laboratorio
Per lavorare con quantità misurabili si utilizza la grandezza grammi per mole (g/mol). Qui entra in gioco il concetto di mole, che rappresenta un numero fisso di particelle, circa 6,022×10²³ (numero di Avogadro).
In pratica, la massa in u di un singolo atomo o molecola diventa direttamente la massa in grammi di una mole di quella sostanza.
Ad esempio, un atomo di carbonio pesa 12 u, quindi una mole di carbonio pesa 12 g; un atomo di ossigeno pesa 16 u, quindi una mole di ossigeno pesa 16 g e così via.
Questo sistema è molto pratico perché i chimici possono usare bilance comuni e calcolare quantità precise di reagenti e prodotti nelle reazioni chimiche.
Come calcolare la massa molecolare
La massa molecolare di una molecola si ottiene sommando le masse atomiche di tutti gli atomi che la compongono. Di seguito sono riportati alcuni esempi:
-
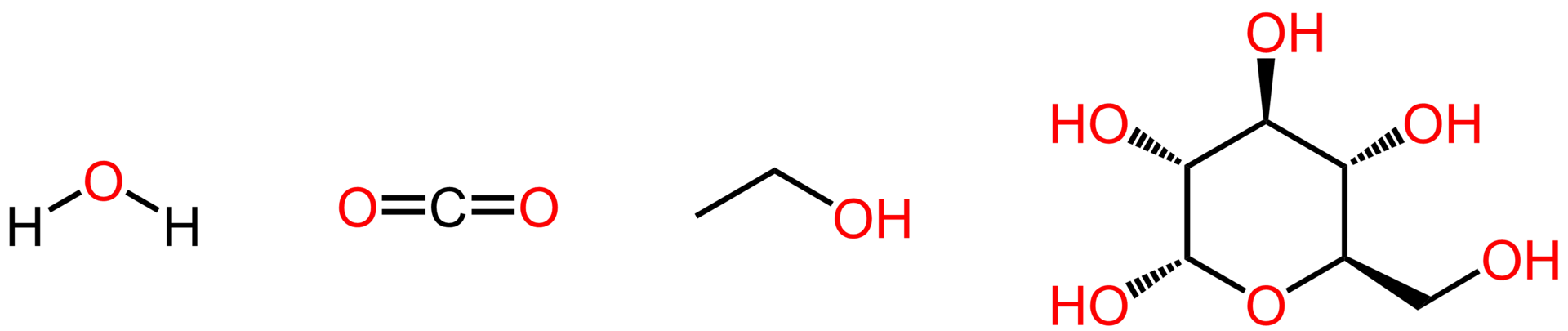
Acqua (H₂O): 2×1 + 16 = 18 u → 18 g/mol
-
Anidride carbonica (CO₂): 12 + 2×16 = 44 u → 44 g/mol
- Etanolo (C₂H₆O): 2×12 + 6×1 + 16 = 46 u → 46 g/mol
-
Glucosio (C₆H₁₂O₆): 6×12 + 12×1 + 6×16 = 180 u → 180 g/mol
Per mettere in pratica quanto appreso, puoi calcolare la massa molecolare delle seguenti sostanze comuni e verificare il tuo risultato con un calcolatore di massa molecolare:
-
Cloruro di sodio (NaCl), anche detto sale da cucina
-
Acido citrico (C₆H₈O₇), presente negli agrumi
-
Lattosio (C₁₂H₂₂O₁₁), presente nel latte
-
Anidride solforosa (SO₂), presente nei vini
-
Acetone (C₃H₆O), usato nei solventi domestici
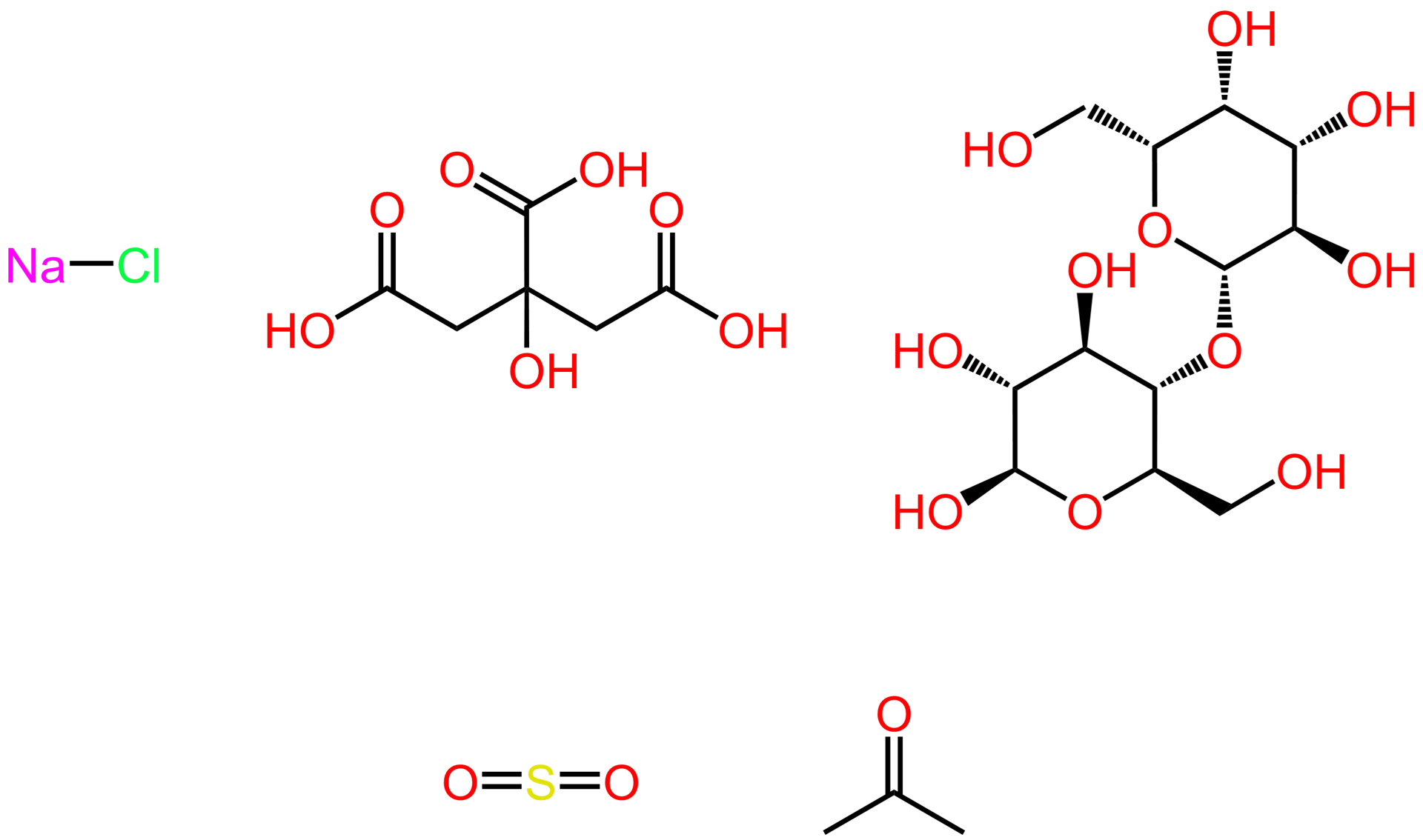
(seconda riga) anidride solforosa, acetone.
Comprendere i concetti di u e g/mol ci permette di collegare formule chimiche, quantità in laboratorio e situazioni della vita quotidiana. Dalla preparazione di una soluzione alla comprensione degli zuccheri negli alimenti, dalla plastica nei materiali di uso comune fino ai solventi domestici, conoscere queste grandezze rende la chimica concreta, tangibile e vicina alla vita reale.
Riassumendo
-
La massa di un atomo si misura in unità di massa atomica (u), utile per confrontare atomi e molecole tra loro.
-
La massa di una mole di sostanza si misura in grammi per mole (g/mol), utile per lavorare con quantità reali in laboratorio.
-
Il peso molecolare si calcola sommando le masse atomiche dei componenti della molecola.
-
Il concetto di mole permette di mettere in relazione i numeri microscopici degli atomi alle quantità macroscopiche che possiamo pesare e usare nella vita quotidiana.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- 1) Petrucci, F. Geoffrey Herring, Jeffry D. Madura e Carey Bissonnette, "Chimica Generale - Principi ed applicazioni moderne", 2025, Piccin Nuova Libraria s.p.a, Padova.



