
Francesco Sbalchiero
Professore di chimica industriale, chimica organica, chimica analitica, chimica inorganica, chimica-fisica. Proprietar…

Molte reazioni chimiche non procedono fino al completo consumo dei reagenti, ma si arrestano quando il sistema raggiunge una condizione di equilibrio. Questo fenomeno, noto come equilibrio chimico, è fondamentale in chimica-fisica, nell’industria chimica e nei processi naturali, perché determina le quantità finali delle specie coinvolte. Comprendere cosa significa il concetto di "equilibrio dinamico", come si definisce la "costante di equilibrio" e in che modo fattori come temperatura e pressione influenzano le reazioni è essenziale per interpretare il comportamento dei sistemi chimici.
In questo articolo analizzeremo il concetto di equilibrio chimico attraverso esempi sperimentali classici, collegandolo ai principi termodinamici che ne governano l’evoluzione.
Equilibrio dinamico ed equilibrio di fase
Consideriamo una trasformazione fisica. Se mettiamo dei cubetti di ghiaccio in un bicchiere d’acqua, osserviamo due fenomeni apparentemente opposti: il ghiaccio fonde, ma contemporaneamente alcuni cubetti si saldano tra loro perché una parte dell’acqua solidifica. In queste condizioni, infatti, il passaggio dallo stato solido a quello liquido e viceversa avviene continuamente, Figura 1.

I fisici e i chimici descrivono questa situazione come un equilibrio dinamico fra stato solido e liquido: le molecole di ghiaccio H₂O(s) passano allo stato liquido, bilanciate da altrettante molecole di acqua H₂O(l) che solidificano.
Un sistema è in equilibrio dinamico quando le velocità delle trasformazioni opposte sono uguali, Figura 2.
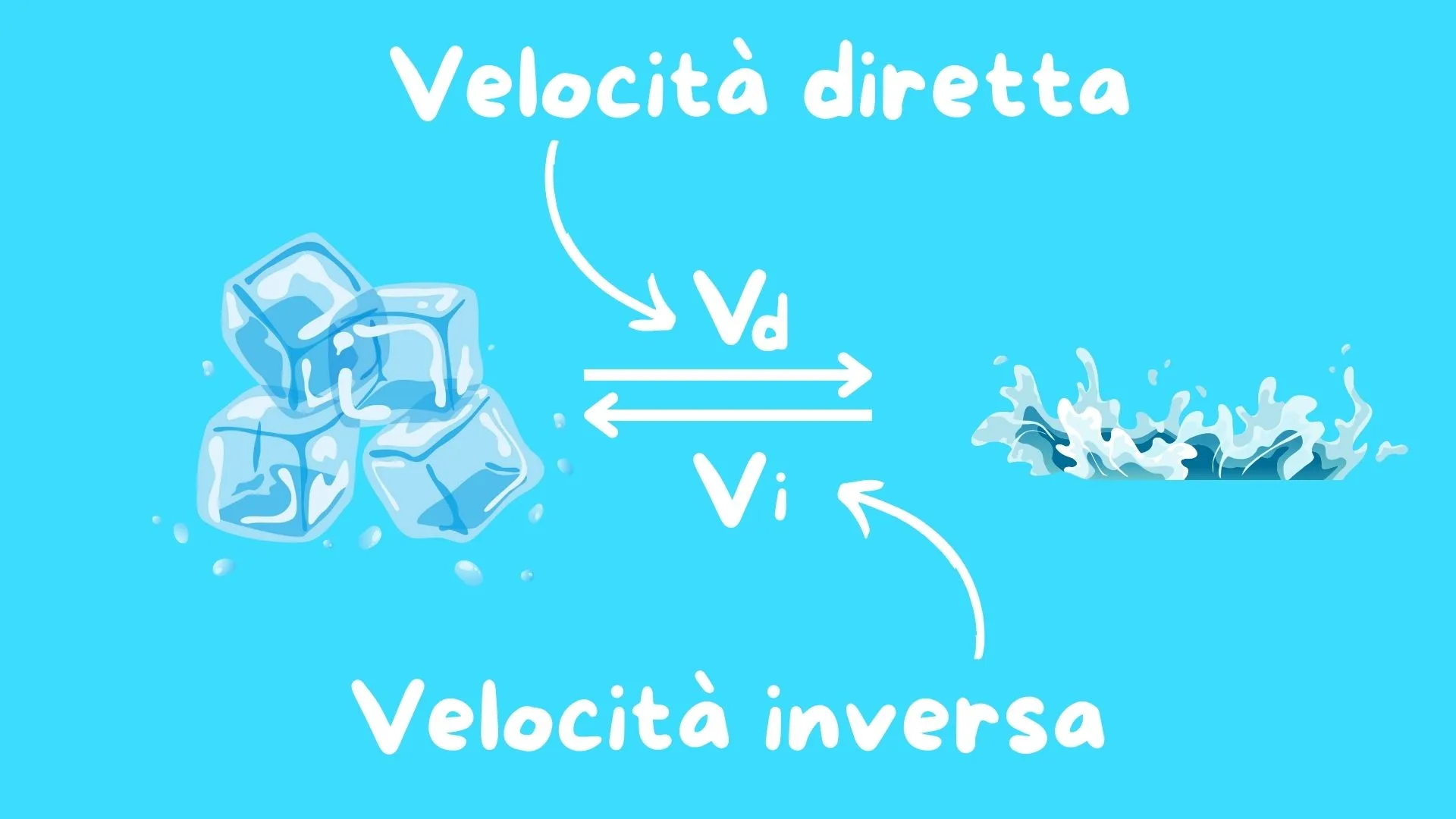
inversa
Questo tipo di equilibrio, che coinvolge il passaggio di stato, è detto equilibrio di fase ed è rappresentato con una doppia freccia, Figura 3.

Equilibrio chimico e sistemi chiusi
L’equilibrio dinamico può instaurarsi anche durante una trasformazione chimica: in questo caso, a sinistra compaiono i reagenti e a destra i prodotti, dando origine a un equilibrio chimico. Tali situazioni non sono molto frequenti in natura perché richiedono sistemi chiusi, privi di scambi di materia con l’esterno, e mantenuti a temperatura costante. Finché queste condizioni sono garantite, il sistema rimane all’equilibrio e non si osservano variazioni macroscopiche. Tuttavia, a livello microscopico, le trasformazioni diretta e inversa continuano ad avvenire incessantemente con la stessa velocità.
Il caso dello ioduro di idrogeno
In laboratorio le reazioni chimiche avvengono spesso in sistemi che possono essere considerati chiusi. Supponiamo di introdurre ioduro di idrogeno gassoso in un pallone di vetro fino a ottenere una concentrazione iniziale di 1 M. A temperatura ambiente (298 K) gli urti tra le molecole non sono sufficienti a superare l’energia di attivazione e la reazione non avviene. A 700 K, invece, si osserva la decomposizione, Figura 4:

Con il tempo compaiono idrogeno e iodio molecolare, quest’ultimo riconoscibile per la colorazione violacea. Man mano che i prodotti si accumulano, però, essi reagiscono tra loro formando nuovamente HI. Dopo un certo intervallo di tempo, la velocità della reazione diretta diventa uguale a quella inversa: le concentrazioni delle specie restano costanti e il sistema ha raggiunto l’equilibrio chimico. Le concentrazioni all’equilibrio dipendono dalle condizioni iniziali, dalla pressione e dalla temperatura.
È importante non confondere l’equilibrio chimico con una situazione di inerzia dovuta all’impossibilità di superare l’energia di attivazione: ad esempio, una miscela di N₂ e O₂ non è in equilibrio, anche se le concentrazioni restano costanti, perché la reazione non parte spontaneamente.
La costante di equilibrio e la legge di azione di massa
Nel 1864 Guldberg e Waage osservarono che, all’equilibrio, esiste un rapporto costante tra le concentrazioni dei prodotti e quelle dei reagenti, ciascuna elevata al proprio coefficiente stechiometrico, Figura 5.

dello ioduro di idrogeno
Questa relazione è una conseguenza della legge di azione di massa, secondo cui, a temperatura e pressione costanti, il rapporto tra il prodotto delle concentrazioni molari dei prodotti e quello dei reagenti, elevati ai rispettivi coefficienti stechiometrici, è costante.
La grandezza di Keq indica quanto la reazione sia spostata verso i prodotti: un valore molto grande segnala un equilibrio a destra, Keq ≈ 1 indica quantità simili di reagenti e prodotti, mentre un valore molto piccolo corrisponde a un equilibrio spostato a sinistra. Nelle reazioni gassose la costante può essere espressa anche in termini di pressioni parziali e viene indicata con Kp.
Energia libera ed equilibrio
Dal punto di vista energetico, una reazione tende a procedere verso la direzione in cui si formano legami più stabili (ΔH < 0) e aumenta il disordine (TΔS > 0). All’equilibrio si ha un bilanciamento tra questi due fattori e vale la relazione:
$$ \Delta G = \Delta H - T \Delta S = 0 $$
In tale condizione l’energia libera di Gibbs assume un valore minimo e non esiste una direzione favorita: il sistema non trae vantaggio né dal formare ulteriori prodotti né dal rigenerare i reagenti.
Effetto della temperatura sull’equilibrio
Il valore della costante di equilibrio varia con la temperatura. Un esempio classico è l’equilibrio tra il tetraossido di diazoto incolore e il diossido di azoto rosso:
$$ \mathrm{N_2O_4(g)} \rightleftharpoons 2\,\mathrm{NO_2(g)} $$
Se una fiala contenente la miscela viene immersa in acqua bollente, la colorazione rossa si intensifica, segnalando un aumento della concentrazione di NO₂. Raffreddando la fiala in acqua e ghiaccio, invece, la miscela diventa più chiara, indicando che l’equilibrio si sposta verso N₂O₄. Questo dimostra come temperatura ed equilibrio siano strettamente collegati.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- Canale YouTube Frank Explains: https://youtu.be/-dONguntgQE?si=bbDUkr5hm90Sgusg



