Pietro Leone Germano
Chimico Industriale laureato all'Università di Padova. Mi piace insegnare e crescere insieme alle persone che mi circon…

Le fasi della materia rappresentano uno dei concetti fondamentali della chimica e della fisica. Ogni sostanza, pura o in miscela, può trovarsi in diversi stati di aggregazione della materia: solido, liquido o gassoso.
Comprendere gli stati della materia e i relativi passaggi di stato permette di spiegare fenomeni quotidiani e processi industriali, oltre a fornire una base essenziale per la termodinamica e la chimica fisica.
Cosa sono le fasi della materia
Le fasi della materia descrivono il modo in cui atomi e molecole si organizzano e si muovono. Nei passaggi di stato non cambia la composizione chimica della sostanza, ma solo la disposizione e l’energia delle particelle.
Le condizioni di una fase sono determinate da tre grandezze fisiche fondamentali: volume (V), pressione (P) e temperatura (T).
Il volume si misura in metri cubi (m³) o litri (L) e rappresenta lo spazio occupato. La pressione, espressa in pascal (Pa) o bar, è definita come:
dove F è la forza (in newton) e A l’area (in m²).
La temperatura, misurata in kelvin (K), è direttamente collegata all’energia cinetica media delle particelle attraverso la costante di Boltzmann (kB). A livello microscopico, questa relazione è espressa da:
$$ E_k = \frac{3}{2} k_B T $$
Queste tre variabili determinano lo stato fisico della materia e il comportamento delle particelle.
Stati di aggregazione della materia: solido, liquido e gas
Gli stati di aggregazione della materia si distinguono per il grado di libertà delle particelle e per l’intensità delle interazioni intermolecolari.
$$ f = 3N - k $$dove:
-
N è il numero di particelle
-
k è il numero di vincoli
Nel solido, le particelle sono fortemente legate e possono solo vibrare attorno a posizioni fisse. Questo comporta un sistema con forma e volume definiti.
Nel liquido, le particelle restano vicine ma sono libere di muoversi e scorrere. Il volume rimane costante, mentre la forma dipende dal contenitore.
Nel gas, le particelle sono completamente libere e il sistema non ha né forma né volume propri. Il comportamento dei gas è descritto dall’equazione dei gas ideali:
$$ PV = nRT $$Questa equazione mette in relazione pressione (Pa), volume (m³), temperatura (K) e quantità di sostanza (mol), ed è fondamentale per comprendere il comportamento della fase gassosa.
Un esempio tipico degli stati della materia è l’acqua: ghiaccio (solido), acqua liquida e vapore (gas). In tutti i casi la sostanza è sempre H₂O, ma cambia il modo in cui le molecole si muovono.
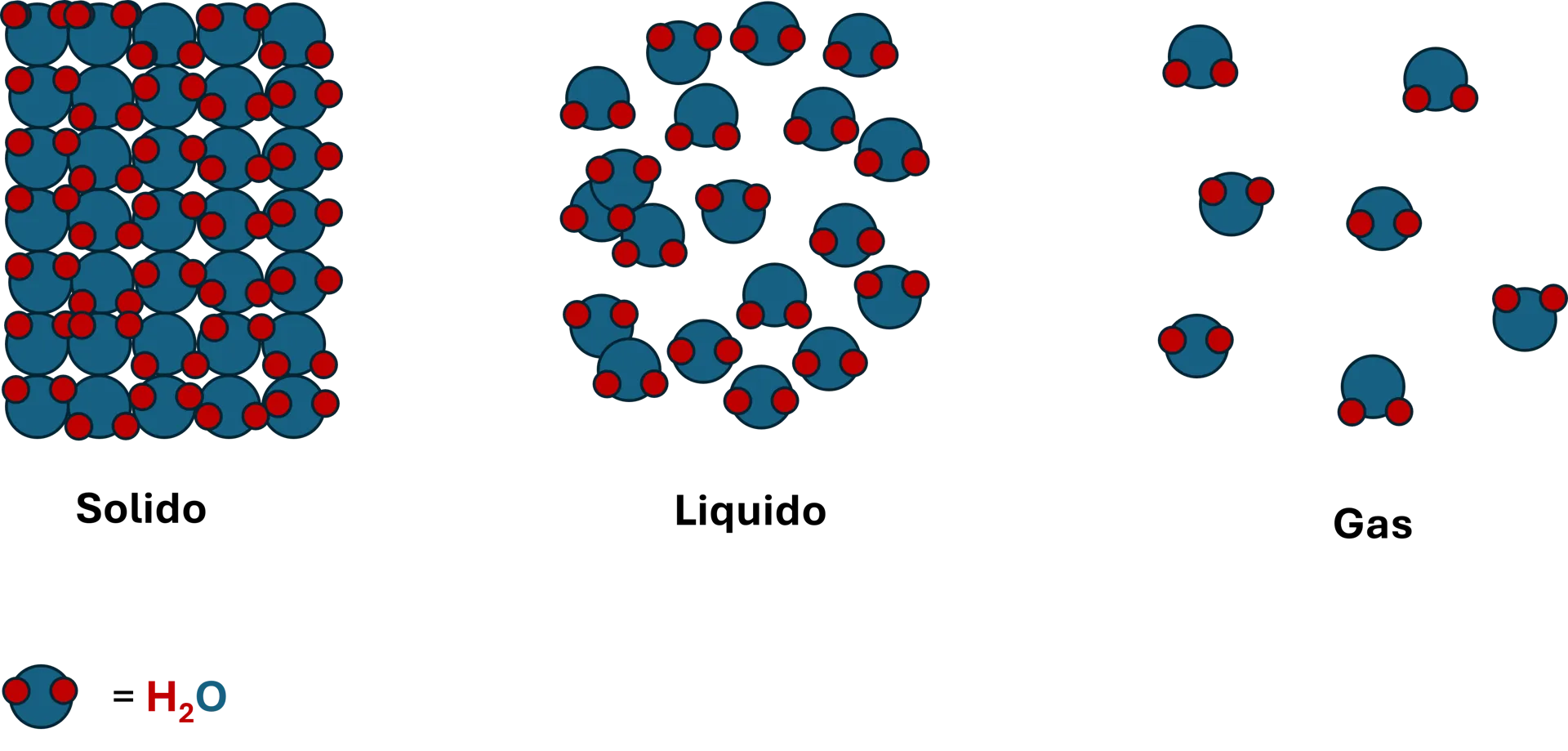
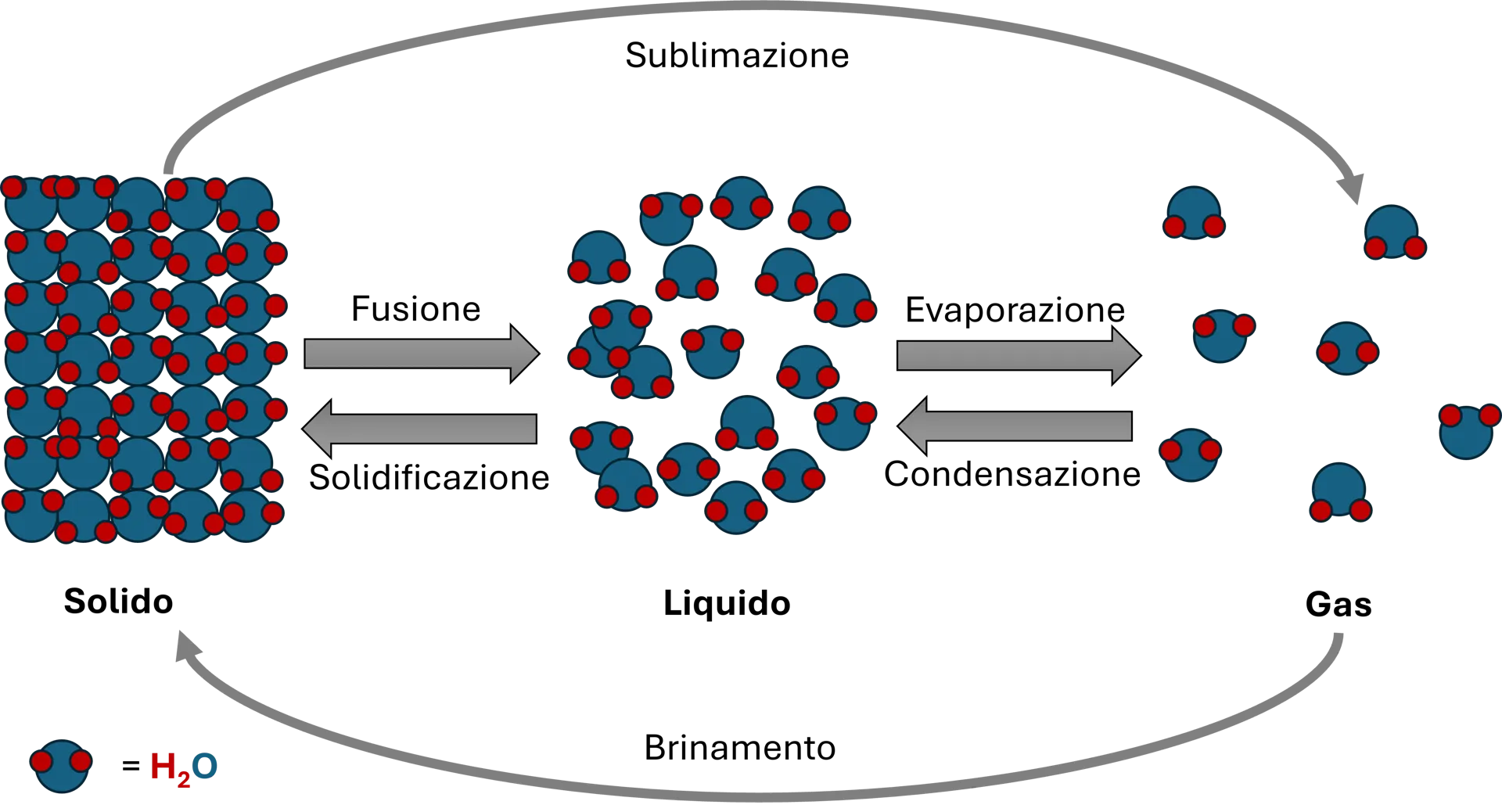
Passaggi di stato della materia
I passaggi di stato avvengono quando variano temperatura e pressione, modificando l’equilibrio tra energia cinetica e forze intermolecolari.
La relazione tra pressione e volume a temperatura costante è descritta dalla legge di Boyle:
$$ PV = \text{cost} $$Questa legge mostra che pressione e volume sono inversamente proporzionali.
Il legame tra volume e temperatura a pressione costante è invece descritto dalla legge di Charles:
$$ \frac{V}{T} = \text{cost} $$A questa si affianca la legge di Gay-Lussac, che descrive la relazione tra pressione e temperatura a volume costante:
$$ \frac{P}{T} = \text{cost} $$Questa relazione indica che, mantenendo costante il volume, la pressione di un gas è direttamente proporzionale alla temperatura assoluta (in kelvin). In termini microscopici, ciò avviene perché un aumento della temperatura incrementa l’energia cinetica delle particelle, che urtano più frequentemente e con maggiore intensità le pareti del contenitore.
Nel complesso, queste leggi spiegano i principali passaggi di stato della materia. Un aumento della temperatura o una diminuzione della pressione favoriscono il passaggio allo stato gassoso, mentre condizioni opposte favoriscono stati più ordinati come liquidi e solidi.
Equilibrio di fase e diagrammi di fase
Le fasi della materia possono coesistere in determinate condizioni di temperatura (K) e pressione (Pa). Questo fenomeno è noto come equilibrio di fase.
Un esempio classico è la coesistenza di ghiaccio e acqua liquida a 0 °C e 1 atm. In queste condizioni, le trasformazioni avvengono in entrambe le direzioni alla stessa velocità.
I diagrammi di fase, come quello riportato sotto per l'acqua, rappresentano graficamente lo stato della materia in funzione di temperatura e pressione.
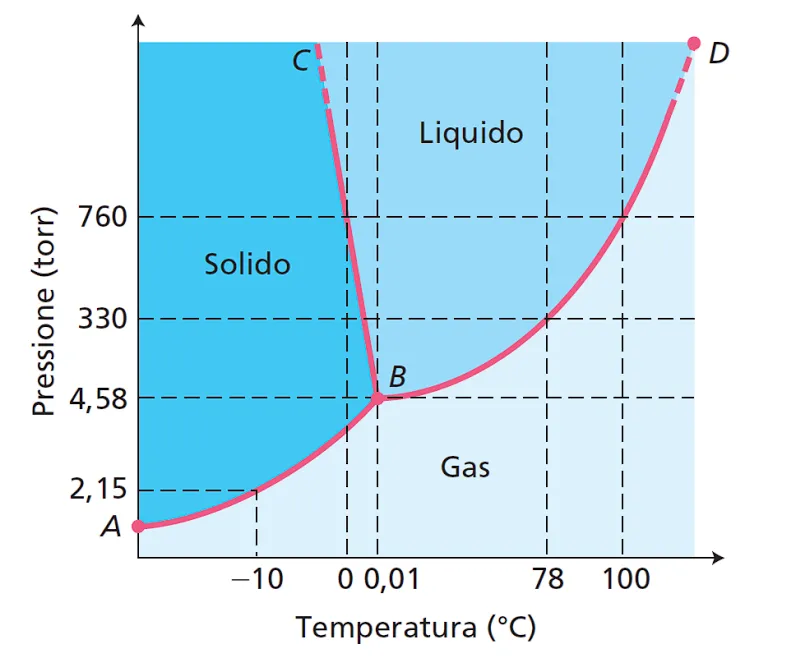
Sull’asse orizzontale è riportata la temperatura (°C), mentre sull’asse verticale è indicata la pressione (torr, mmHg).
Le linee di confine tra le fasi rappresentano le condizioni di equilibrio tra stati. Il punto in cui le tre linee si incontrano è il punto triplo, dove ghiaccio, acqua e vapore coesistono contemporaneamente. Il punto critico, invece, delimita la temperatura e pressione oltre le quali il liquido e il gas non sono distinguibili.
Per concludere, le fasi della materia dipendono dal comportamento delle particelle e dal loro grado di libertà. Le grandezze fondamentali sono volume (m³), pressione (Pa) e temperatura (K), legate tra loro dalle relazioni esposte sopra.
Quando queste variabili cambiano, si verificano i passaggi di stato, che trasformano la materia tra solido, liquido e gas senza modificarne la composizione chimica.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- 1) Petrucci, R. H., Herring, F. G., Madura, J. D., & Bissonnette, C. (2014). Chimica generale. Principi ed applicazioni moderne (10ª ed.). Piccin‑Nuova Libraria. ISBN 978‑8829926923.