
Francesco Sbalchiero
Professore di chimica industriale, chimica organica, chimica analitica, chimica inorganica, chimica-fisica. Proprietar…

Tra i composti più estremi conosciuti dalla chimica, l’acido fluoroantimonico (HSbF₆) occupa un posto speciale. Si tratta di uno dei cosiddetti superacidi, ossia acidi molto più forti dell’acido solforico puro (H₂SO₄). La sua forza è tale da poter protonare anche gli idrocarburi, sostanze normalmente considerate quasi impossibili da acidificare.
Cos’è l’acido fluoroantimonico
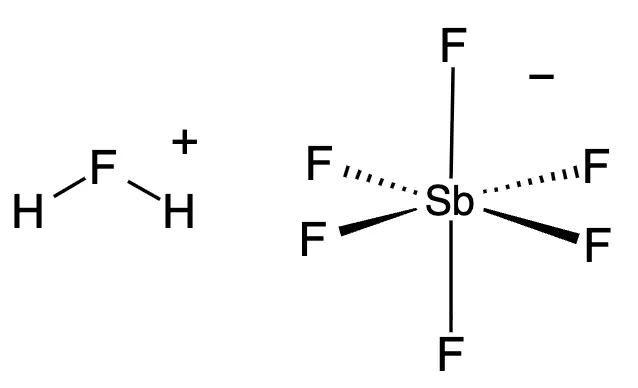
L’acido fluoroantimonico, chiamato anche acido esafluoroantimonico, è una miscela in rapporto 1:1 di acido fluoridrico (HF) e pentafluoruro di antimonio (SbF₅).
La reazione tra queste due sostanze è estremamente esotermica:
HF + SbF₅ → H⁺ + SbF₆⁻
Durante la reazione, l’acido fluoridrico cede un protone (H⁺) e il suo anione (F⁻) viene catturato da SbF₅, formando l’anione esafluoroantimonato (SbF₆⁻). Questo anione è non coordinante, cioè molto stabile, con bassa capacità di reagire o stabilizzare il protone.
Il risultato è un sistema in cui il protone rimane quasi “nudo”, cioè poco schermato dalle cariche negative circostanti.
È proprio questa condizione a rendere l’acido fluoroantimonico oltre 2×10¹⁹ volte più forte dell’acido solforico concentrato — una differenza immensa, che lo colloca ai vertici della scala dell’acidità conosciuta.
La sintesi dell’acido fluoroantimonico richiede attrezzature specializzate e condizioni di massima sicurezza.
La reazione diretta tra HF e SbF₅ produce gas tossici e vapori corrosivi, ed è condotta esclusivamente in laboratori altamente attrezzati, sotto cappa aspirante e con materiali resistenti alla corrosione. A causa della sua pericolosità, questo composto non è mai preparato o manipolato al di fuori di strutture di ricerca avanzata.

Effetti sull’uomo e rischi
L’acido fluoroantimonico è uno dei composti più corrosivi esistenti.
Il contatto con la pelle o con i tessuti biologici causa danni immediati, necrosi profonda e rilascio di gas tossici.
L’inalazione dei vapori provoca lesioni gravi alle vie respiratorie e ai polmoni. Per questi motivi, la manipolazione richiede dispositivi di protezione avanzati: guanti speciali, visiere, tute resistenti agli acidi e una cappa aspirante idonea.
Perché l’acido fluoroantimonico non ha un pH: la funzione di Hammett
L’acido fluoroantimonico è così forte che non può essere descritto dalla normale scala del pH.
Per quantificare l’acidità di acidi molto concentrati o superacidi, i chimici usano la funzione di acidità di Hammett (H₀), introdotta da Louis Plack Hammett.
Questa funzione estende il concetto di pH a soluzioni non acquose o estremamente concentrate, dove il pH classico perde significato.
Un acido è tanto più forte quanto più negativo è il suo valore di H₀.
Ad esempio:
-
Acido solforico concentrato → H₀ = –12
-
Acido fluoroantimonico → H₀ ≈ –28
Un valore così basso non significa che la concentrazione di ioni H₃O⁺ sia reale, ma indica una capacità protonante equivalente a una concentrazione “virtuale” di protoni altissima.
Applicazioni e utilizzi
Nonostante la sua pericolosità, l’acido fluoroantimonico ha importanti applicazioni scientifiche.
È utilizzato in ricerche di chimica avanzata, in particolare per:
-
stabilizzare cationi estremamente instabili,
-
catalizzare reazioni che richiedono ambienti fortemente protonanti,
-
sintetizzare composti organici complessi,
-
e studiare i limiti della chimica acido-base.

Il suo impiego è limitato a pochi laboratori altamente specializzati, che ne sfruttano la potenza per esplorare nuovi campi della chimica fondamentale.
L’acido fluoroantimonico rappresenta uno dei limiti estremi della chimica moderna: potentissimo, instabile e pericoloso, ma anche fondamentale per la ricerca.
È un perfetto esempio di come la chimica riesca a spingersi ai confini della materia, rivelando fenomeni altrimenti inaccessibili.
Naturalmente, si tratta di un composto da non maneggiare mai al di fuori di un laboratorio attrezzato.
La sua potenza è affascinante proprio perché resta confinata al mondo della ricerca avanzata dove scienza e prudenza vanno sempre di pari passo.
Ti è piaciuto l'articolo?
Salvalo nei preferiti o condividilo con altri appassionati!
Fonti
- Olah, G. A., Prakash, G. K. S., & Sommer, J. (1985). Superacids. Wiley-Interscience.
- Wiberg, E., & Holleman, A. F. (2001). Inorganic Chemistry. Academic Press.
- Edwards, H. G. M., & Chalmers, J. M. (2005). Handbook of Vibrational Spectroscopy. Wiley.
- https://www.acs.org/molecule-of-the-week/archive/f/fluoroantimonic-acid.html
- Canale YouTube "Frank explains": https://www.youtube.com/watch?v=dLsjIYXM_1k?sub_confirmation=1

